រូបទី 1៖ យន្តហោះនៅរយៈកម្ពស់ដ៏ខ្ពស់មួយ (កម្រិតអុកស៊ីសែនទាប)
——–
អ្នកទាំងអស់គ្នាប្រហែលជាធ្លាប់ឃើញតាមកញ្ចក់ទូរទស្សន៍ឬដោយផ្ទាល់ហើយបើធ្លាប់ធ្វើដំណើរតាមជើងអាកាសថាក្នុងពេលមានអាសន្នដូចជាពេលដែលយន្តហោះមានបញ្ហានៅពេលវានៅរយៈកម្ពស់ខ្ពស់មួយដែលកម្រិតអុកស៊ីសែនមានកម្រិតទាបនោះអ្នកដំណើរទាំងអស់ត្រូវបានបុគ្គលិកបម្រើការលើយន្តហោះណែនាំឲ្យពាក់ស្រោមមុខដែលធ្លាក់ចុះពីពិដានរបស់តួរយន្តហោះខាងក្នុងដើម្បីអនុញ្ញាតឲ្យអ្នកដំណើរអាចប្រើអុកស៊ីសែននោះសម្រាប់ដកដង្ហើម។
យោងតាមសមត្ថកម្មខាងលើថ្ងៃនេះ «គំនិត» ចង់សួរអ្នកទាំងគ្នាថាអ្នកយល់យ៉ាងដែរចំពោះប្រភពនៃឧស្ម័នអុកស៊ីសែនទាំងនោះ? តើក្រុមហ៊ុនអាកាសចរណ៍ត្រូវដឹកឧស្ម័នទាំងនោះក្នុងស៊ីទែនផ្ទុកមួយក្នុងយន្តហោះនោះមែនទេ?
បើអ្នកទាំងអស់គ្នាឆ្លើយថានៅលើយន្តហោះមានផ្ទុកឧស្ម័នអុកស៊ីសែនអ្នកប្រហែលជាភ្លេចថាការដឹកជញ្ជូនឧស្ម័នមានផលលំបាកធំមួយគឺគ្រោះថ្នាក់ជាយថាហេតុផ្សេងៗដោយសារឧស្ម័ននៅពេលទទួលកម្តៅវារីកមាឌ។ការរីកមាឌនេះអាចបណ្តាលឲ្យកើតនូវបាតុភូតមួយហៅថា«បន្ទុះ»។ ម្យ៉ាងទៀតយន្តហោះដែលចំណាយឥន្ធនៈតិចត្រូវតែមានទម្ងន់ស្រាល។ បើស្ថាបត្យករសម្រេចដឹកឧស្ម័ននោះគេត្រូវបង្កើតស៊ីទែនធំនិងក្រាស់មួយដើម្បីការពារបាតុភូតបន្ទុះដូចពន្យល់ខាងលើ។ ដូចនេះបើយន្តហោះមិនមានផ្ទុកស៊ីទែនអ៊ុកស៊ីសែនទេនោះតើគេបានអ៊ុកស៊ីសែនពីណាមក?
បើអ្នកទាំងអស់គ្នាមានចម្ងល់សូមមកចូលរួមអានអត្ថបទខាងក្រោមទាំងអស់គ្នា។(សូមមើលរូបខាងក្រោមដែលជារចនាបទទូទៅមួយនៃយន្តហោះទាំងមូល)

រូបទី 2៖ រចនាបទ (ទូទៅ) នៃតួរយន្តហោះ
——-
ដូចបានរៀបរាប់ខាងលើការដឹកជញ្ជូនឧស្ម័នមានផលលំបាកធំមួយគឺគ្រោះថ្នាក់ដោយបន្ទុះដូចនេះស្ថាបត្យករយន្តហោះបានរុករកវិធីផ្សែងទៀតដែលអាចដឹកជញ្ជូនឧស្ម័នអុកស៊ីសែនជាទម្រង់អង្គធាតុរឹងហើយឧស្ម័នអុកស៊ីសែននឹងត្រូវបង្កើតឡើងនៅពេលដែលត្រូវការតែប៉ុណ្ណោះ។អ្វីដែលអនុញ្ញាតឲ្យស្ថាបត្យករយន្តហោះអាចសម្រេចបំណងនោះបានគឺរបកគំហើញផ្នែកគីមីវិទ្យាមួយគឺប្រតិកម្មចំហេះនៃសារធាតុម្យ៉ាងដែលចាត់ចូលក្នុងក្រុមក្លរាត់(ClO3– ) ។
រូបទី 3៖ អំបិលក្លរាត
—–
នៅពេលដែលអំបិលនៃក្រុមក្លរាត់នេះប៉ះទៅនឹងកម្តៅខ្លាំងឬអណ្តាតភ្លើងវានឹងឆាបឆេះហើយបញ្ចេញនូវឧស្ម័នអុកស៊ីសែន។ តាមទិន្នន័យដែលគេទទួលបានពីក្រុមហ៊ុនផលិតយន្តហោះអុកស៊ីសែនដែលបង្កើតតាមរយៈប្រតិកម្មនេះគ្រប់គ្រាន់សម្រាប់អ្នកដំណើរក្នុងរយៈពេល១៥នាទី(គ្រប់គ្រាន់សម្រាប់យន្តហោះបន្ទាបខ្លួនមករយៈកម្ពស់ល្មមដែលមានកម្រិតអុកស៊ីសែនធម្មតា)។
—–
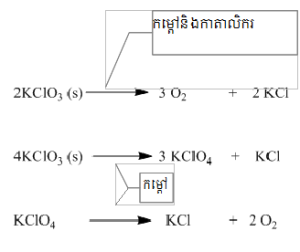
ប្រតិកម្មទី 1 គឺជាប្រតិកម្មចំហេះដែលមានកាតាលិករដូចនេះអុកស៊ីសែនត្រូវបានបង្កើតឡើងនៅតំណាក់កាលទី 1 តែម្តង។
ប្រតិកម្មទី 2 និងទី 3 គឹប្រតិកម្មដែលកើតឡើងដោយគ្មានកាតាលិករគឺត្រូវឆ្លងកាត់ការដុត 2 តំណាក់កាលដើម្បីបង្កើតអុកស៊ីសែន។
សូមមើល វីដេអូនៃការដុត KClO3 ខាងក្រោម
—————
នៅតាមយន្តហោះស្រោមមុខអុកស៊ីសែនដែលធ្លាក់ពីពីដាននោះត្រូវបានតភ្ជាប់ទៅនឹងកុងតាក់ដែលធ្វើឲ្យមានបន្ទុះតូចមួយដែលជាបុព្វហេតុនៃចំហេះរបស់ផ្សៅដែកដែលគេផ្សំនឹងម្សៅសូដ្យូមក្លរាត (NaClO3) ឬ ប៉ូតាស្យូមក្លរាត (KClO3)។ ក្រោយចំហេះទាំងនេះដែក (៣)អុកស៊ីតសូមដ្យូមឬប៉ូតូស្យូមក្លរួនិងអុកស៊ីសែនត្រូវបានបង្កើតឡើង។
ទោះជាស្ថាបត្យករយន្តហោះទស្សន៍ទាយថាការបង្កើតអុកស៊ីសែនតាមវិធីនេះមានសុវត្ថិភាពជាងការដឹកជញ្ជូនឧស្ម័នដោយផ្ទុកវាក្នុងស៊ីទែនឧបត្ថវហេតុ (២ទៅ៣ករណីយ) ដែលបង្កឡើងដោយប្រតិកម្មនេះត្រូវបានគេរាយការតែបើយើងប្រៀបធៀបគ្រោះថ្នាក់នៃការដឹកជញ្ជូនឧស្ម័នផ្ទាល់នោះវាអាចបង្ករគ្រោះថ្នាក់ច្រើនករណីយជាងនេះទៅទៀត។
ជាទីបញ្ចប់ «គំនិត» គ្រាន់តែចង់បណ្តុះគំនិតអ្នកអានទាំងអស់ឲ្យងាកមកចាប់អារម្មណ៍លើផ្នែកវិទ្យាសាស្រ្តព្រោះបើយើងគិតឲ្យដល់ទៅបើអ្នកប្រាជ្ញមិនបានរកឃើញនោះក៏យើងគ្មានរបកគំហើញផ្នែកបច្ចេកវិទ្យាដែរ។
វីដេអូនៃការដុត KClO3
ដកស្រង់ចេញពី
http://en.wikipedia.org/wiki/Potassium_chlorate
http://en.wikipedia.org/wiki/Emergency_oxygen_system
រូបភាព
ទី1៖http://www.greenbang.com/wp-content/uploads/2009/06/airbus.jpg
ទី3៖http://www.vk2zay.net/article/file/265
ទី4៖http://www.dvorak.org/blog/wp-content/uploads/2011/03/airplaneoxygenmask.jpg